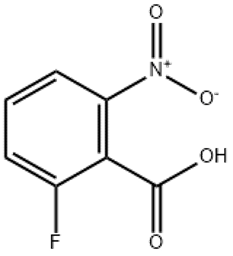
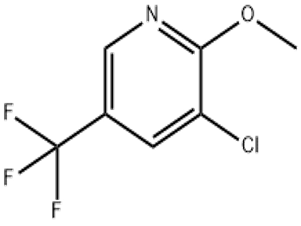
2,4-Dichloronitrobenzène (CAS#611-06-3)
| Symboles de danger | Xn – NocifN – Dangereux pour l’environnement |
| Codes de risque | R21/22 – Nocif par contact avec la peau et par ingestion. R43 – Peut entraîner une sensibilisation par contact avec la peau R51/53 – Toxique pour les organismes aquatiques, peut entraîner des effets néfastes à long terme pour l'environnement aquatique. |
| Description de la sécurité | S24 – Éviter le contact avec la peau. S36/37 – Porter des vêtements et des gants de protection appropriés. S61 – Éviter le rejet dans l'environnement. Se référer aux instructions spéciales/fiches de données de sécurité. |
Introduction
Le 2,4-dichloronirobenzène est un composé organique de formule chimique C6H3Cl2NO2. C'est un cristal jaune avec une odeur âcre.
L’une des principales utilisations du 2,4-dichloronirobenzène est celle d’intermédiaire pour les pesticides et les insecticides. Il peut être utilisé pour synthétiser une variété de pesticides et d'herbicides et a un bon effet destructeur sur les ravageurs et les mauvaises herbes. De plus, il peut également être utilisé dans les domaines des colorants, des pigments, de l’industrie pharmaceutique, cosmétique et du caoutchouc.
Le 2,4-dichloronitrobenzène a de nombreuses méthodes de préparation, la plus courante étant obtenue par chloration du nitrobenzène. Dans le processus spécifique, le nitrobenzène réagit d'abord avec du chlorure ferreux pour former du nitrochlorobenzène, puis est chloré pour obtenir du 2,4-dichloronitrobenzène. Le processus de préparation nécessite une attention particulière à la température et aux conditions de réaction.



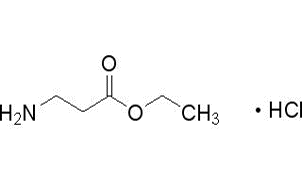

![6-Bromo-7-chloro-3H-imidazo[4 5-b]pyridine (CAS# 83472-62-2)](https://cdn.globalso.com/xinchem/6Bromo7chloro3Himidazo45bpyridine.png)